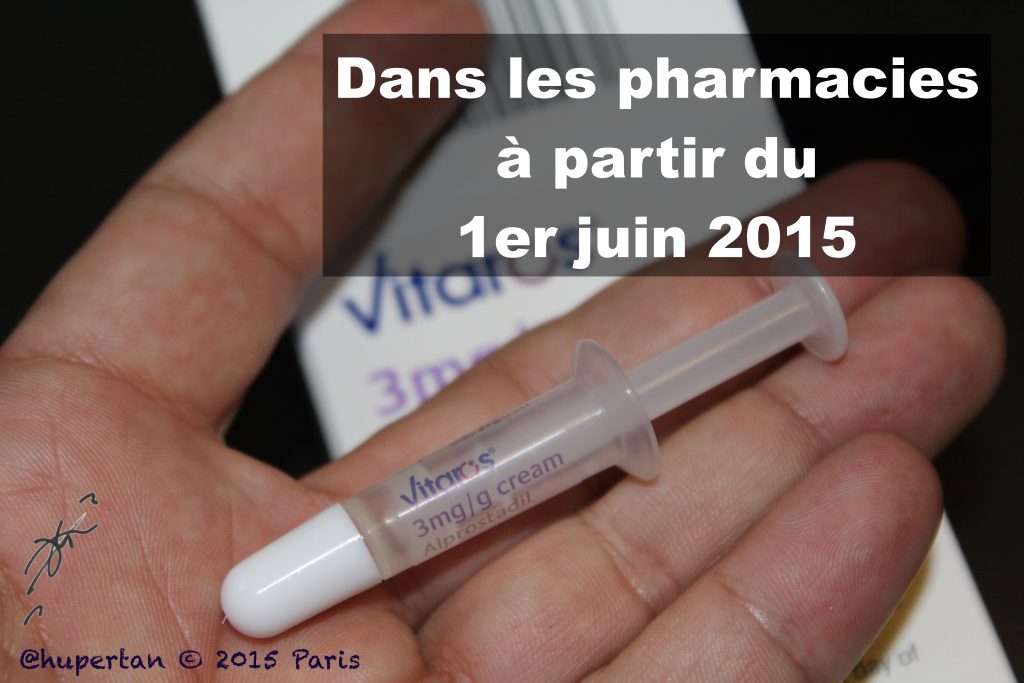
Vitaros crème: à peine disponible en pharmacies, donc aucune expérience de terrains, et le Vitaros fait le Buzz: “crème alternative au Viagra”, “Vitaros crème n’est pas sans risque: priapisme, stérilité, brûlures!
VITAROS, alprostadil sous forme de crème indiquée dans le traitement de la dysfonction érectile n’est pas bien installé dans les pharmacies et l’Internet c’est déjà emballé!
Author: Vincent Hupertan,MD Urologist and Sexologist in Paris creator of http://www.uroblog.fr.
Vitaros est disponible dans les officines françaises depuis le 1er juin 2015.  http://leplus.nouvelobs.com/contribution/1378260-vitaros-nouvelle-alternative-au-viagra-priapisme-sterilite-brulures-c-est-risque.html
http://leplus.nouvelobs.com/contribution/1378260-vitaros-nouvelle-alternative-au-viagra-priapisme-sterilite-brulures-c-est-risque.html
On est plus dans la recherche du scoop que de fournir une information neutre, impartiale et critique. On oublie qu’il s’agit des patients et tous ceux qui donnent leur avis doivent avoir une responsabilité dans l’éducation thérapeutique des lecteurs.
Dans ce petit post je vais donner des données factuelles issues des études cliniques (appelées dans le jargon “essais cliniques randomisée ou de phase IIII») avec des références bibliographiques à l’appui pour étayer ou confirmer des informations, certaines vraies certaines fausses sur les avantages et les inconvénients du VITAROS.
Dans un très joli article intitulé:
” Une crème alternative au Viagra: priapisme, stérilité, brûlure… Ce n’est pas sans risque »
La critique se fait sur le fond et la forme.
Je ne vais pas insister sur l’alternative au Viagra, qui fait l’objet d’un article en cours de rédaction. Je vais insister sur l’approche émotionnelle négative de l’article avec une remarque forte “Ce n’est pas sans risque”.
[tweet https://twitter.com/HUPERTAN/status/606424514449276929 align=’right’]
Sur les risques des produits pharmaceutiques, il n’y a pas lieu à débattre. A titre d’exemple, le Paracétamol, le médicament le plus prescrit en France (nourrissons, femmes enceintes,…) présente un risque négligeable et sous-estimé par les professionnels de santé en terme des effets secondaires.
Si c’est exact que “Ce n’est pas sans risque” fallait-il le mettre en évidence?!
1) Première remarque – “stérilité“
” Une crème alternative au Viagra: priapisme, stérilité, brûlure… Ce n’est pas sans risque »
C’est pour la toute première fois, que je lis ce type d’effet secondaire. Ni dans les publications et encore moins dans cet article. J’invite le journaliste à nous éclairer car c’est une information importante et je souhaiterais avoir cette information.
2) Deuxième, le terme médical « brûlures »
Même si Wikipédia n’est pas une information suffisamment fiable en matière médicale, on peut accepter la définition:
“La brûlure est une destruction partielle ou totale pouvant concerner la peau, les parties molles des tissus, ou même les os.” source http://fr.wikipedia.org/wiki/
Chez la femme il s’agissait “des brûlures vaginales d’intensité légère à modérée” et chez l’homme “principalement d’une sensation de chaleur ou de brûlure dans le pénis” selon L’avis de la Commission de la transparence[…] . On n’a pas besoin d’être médecin ou journaliste pour voir la différence entre les deux
3) Last but not least – “priapism“
C’est un mot fort et tout médecin qui en a rencontré a dû être marque cette situation clinique, une vraie urgence médico-chirurgicale. Dans le même document «L’avis de la Commission de la transparence adopté le 18 février 2015 » de La Haute Autorité De Santé (H A S) la définition du platine est la suivante :
«Priapisme Une érection se prolongeant plus de 4 heures”.
[tweet https://twitter.com/HUPERTAN/status/606434472863625217 align=’right’ width=’200′ ]
L’avis de la Haute Autorité de Santé est basée sur des données issues des 2 études, dites essais cliniques de phase 3, randomisée et en double aveugle, c’est-à-dire que ni les patients ni les médecins n’étaient pas au courant du produit administré. On a comparé le VITAROS avec le PLACEBO. C’est une étude réalisée sur 12 semaines chez des hommes souffrant de dysfonction érectile. Après les 12 semaines les patients avaient la possibilité de continuer on ouvert c’est-à-dire ils étaient au courant du produit administré.
Une première étude:
l’étude MED 2000-004 Au total, 878 patients ont été inclus dans l’étude. Parmi eux, 712 (81 %) ont terminé l’étude.
et une deuxième étude:
étude MED 2000-005 Au total, 854 patients ont été inclus dans l’étude. Parmi eux, 695 (81 %) ont terminé l’étude.
En matière des effets secondaires dans les :
études cliniques MED 2000-004 et 2000-005 Au total, 1 298 patients ont reçu de l’alprostadil à la dose de 100, 200 ou 300 µg dans le cadre des études MED 2000-004 et 2000-005.
il y a eu des:
Réactions locales […] principalement d’une sensation de chaleur ou de brûlure dans le pénis, d’une douleur ou d’un érythème pénien dont l’incidence augmentait avec la dose d’alprostadil administrée. Evénements chez la partenaire L’incidence des réactions vaginales locales chez la partenaire a été de 4 % (15/434) dans le groupe placebo, 5 % (22/434) dans le groupe alprostadil 100 µg, 9 % (37/430) dans le groupe 200 µg et 7 % (30/434) dans le groupe 300 µg. Il s’agissait principalement de brûlures vaginales d’intensité légère à modérée. Priapisme Une érection se prolongeant plus de 4 heures a été observée chez 1 patient dans l’étude MED 2000-005.
En ce qui concerne l’étude ouverte:
l’étude MED 2000-006 L’étude MED 2000-006 est une étude d’extension en ouvert de 12 mois visant à évaluer la tolérance à long terme de l’alprostadil par voie topique. Au total, 1 162 patients ont été inclus (999 patients des études MED 2000-004 et MED 2000-005 et 163 nouveaux patients). Aucun événement indésirable nouveau n’a été identifié.
Au-delà des chiffres
Les études c’est important mais ce n’est pas toute à fait la vraie vie. Il y a la clinique et l’expérience pratique du prescripteur.
À titre personnel durant les 13 ans d’expérience avec l’alprostadil dans sa forme injectable jeune ramait jamais rencontrer du priapisme pour mes patients. Bien que j’ai traité un certain nombre d’autres patients présentant un priapisme.
Ne pas oublier que le VITAROS est un médicament, une spécialité par voie topique à base d’alprostadil dans le traitement de la dysfonction érectile.
En matière de “Conditions de prescription et de délivrance” c’est un médicament inscrit sur la liste I (listes de médicaments en fonction des risques que représente leur prise.). Sa délivrance est soumise à une prescription médicale. Le prescripteur doit tenir compte des Résumé des caractéristiques du produit Par ailleurs comme tout produit existant sur le marché il fait l’objet d’une surveillance de type pharmacovigilance pour évaluer l’apparition des effets secondaires durant la phase d’utilisation des médicaments. Tout médecin qui rencontre un effet secondaire chez ces patients et en particulier avec la piscine est dans l’obligation de signaler et de remplir un dossier ou une fiche signalétique.
En tant que urologues – andrologue – sexologue je considère que la prise en charge de la dysfonction est-il doit être multimodal quel que soit l'origine, psychogène, organiques mais le plus souvent mixte. Ce serait une erreur de limiter la prise en charge à une prescription médicamenteuse et sans accompagnement psycho sexologique tout comme rester sur une approche sexologique pure sans évaluation médicale et en particulier cardio-métabolique. Le diabète, les dyslipidémies ou encore l'hypertension artérielle, pour ne citer que les situations cliniques le plus fréquentes, la dysfonction érectile est un élément clinique majeur.